Avec la multiplication des bactéries résistantes, nombre d’antibiotiques sont devenus inactifs. La situation s’aggrave et la mise au point de molécules innovantes devrait être une priorité. Pourtant la recherche avance peu. Une situation alarmante dénoncée par Patrice Courvalin, de l’Institut Pasteur.

La résistance des bactéries aux antibiotiques est-elle en hausse ?
Patrice Courvalin : Oui, car même si des progrès ont été enregistrés dans certains pays d’Europe et en France en particulier, la prescription d’antibiotiques reste très forte en médecine de ville où encore de nombreux patients considèrent que les antibiotiques sont un passage obligé vers la guérison. Quant à la prescription en milieu hospitalier, elle est devenue raisonnable, prudente, mais reste indispensable dans certaines unités comme les soins intensifs pour sauver des malades. Lorsque j’étais interne dans les années 70, je disposais de beaucoup plus de molécules actives qu’aujourd’hui pour sauver des patients et le phénomène est irréversible. Il est dans la nature même des bactéries de s’échanger des gènes et de muter. Que ce soit de manière aléatoire ou en réponse à des attaques comme celle d’un antibiotique. La prescription intensive d’antibiotiques depuis cinquante ans pour la santé humaine et en élevage animal a sélectionné quantité de souches résistantes contre lesquelles certaines familles d’antibiotiques n’ont plus aucune action. Et l’apparition des multirésistances ou co-résistances, c'est-à-dire des bactéries qui acquièrent la capacité à résister à plusieurs familles d’antibiotiques, fait que le nombre de molécules actives disponibles diminue.
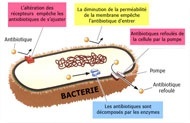
La sélection de souches résistantes par les antibiotiques
Il faut distinguer l’émergence d’une résistance et sa dissémination. L’émergence d’une résistance chez des bactéries est un phénomène naturel qui n’est pas lié à une prescription d’antibiotique. C’est le plus souvent une mutation aléatoire, due au hasard, ou l'acquisition d'un gène de résistance en provenance d'une autre bactérie. La bactérie résistante n’a pas d’avantage compétitif sur les autres bactéries et ne prolifère pas massivement.
C’est au contact d’un antibiotique qu’elle va pouvoir coloniser l’organisme et disséminer. Car pour lutter contre l’infection (rappelons que les antibiotiques ne sont actifs que contre les bactéries et n’ont aucune action sur les virus) l’antibiotique – dont l’action est parfois comparée à celle d’un bulldozer dans un jardin – va éliminer un grand nombre de bactéries et libérer le terrain pour les bactéries résistantes qui vont proliférer dans le milieu.
Est-on aujourd’hui dans une course contre la montre entre l’émergence de ces multirésistances et la conception de nouvelles molécules ?
P.C. : Ce serait vrai si la recherche était mobilisée, mais l’industrie pharmaceutique s’est totalement désengagée depuis plus de dix ans. Pour des raisons qui tiennent principalement à des questions de rentabilité. Les antibiotiques sont des médicaments qui agissent rapidement : une infection urinaire, c’est entre trois et cinq jours de traitement, une méningite bactérienne qui est pourtant une infection sévère, au bout de 24 heures vous voyez si le traitement marche. Et de façon à retarder l’évolution vers la résistance, la tendance est à raccourcir la durée des prescriptions et à augmenter les doses. Les profits sont donc moins importants et les investissements des laboratoires se sont orientés vers les maladies chroniques (Alzheimer, Parkinson…) ou des infections virales comme le sida ou l’hépatite pour lesquelles les patients sont traités sur des années.
La seconde raison est que plus un antibiotique est innovant, moins il va être prescrit pour, là encore, retarder l’évolution vers la résistance. Si vous avez une molécule authentiquement nouvelle, c’est-à-dire active sur des souches résistantes aux autres familles d’antibiotiques, son usage va être réservé à l’hôpital pour ne pas sélectionner et disséminer des résistances. C’est le cas d’un des rares antibiotiques nouveaux, le linézolide qui est prescrit à l’hôpital dans le cas d’infections graves et face à des bactéries résistantes à la méthicilline et aux pénicillines. Il est certes très cher mais ceci ne compense pas le fait que les volumes de prescription sont en ville et pas dans les hôpitaux. Donc tout cela n’est pas très incitatif pour l’industrie pharmaceutique.
En plus la recherche d’antibiotique est difficile, longue, il faut compter dix à douze ans entre la découverte de ce que l’on appelle un « lead », c'est-à-dire une nouvelle molécule, et sa commercialisation.
Quelques chiffres
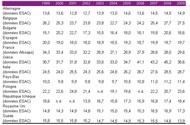
Depuis la campagne « Les antibiotiques, c’est pas automatique » lancée en 2002, la consommation d’antibiotiques en France a baissé de 16%. Ce mouvement de baisse enregistré tant en « ville » qu’à l’hôpital n’a cependant pas été continu et, depuis 2005, la tendance est à une légère reprise. La France a toujours une consommation très supérieure à la moyenne européenne et se situe parmi les pays à très forte consommation.
80% du chiffre d’affaires de la vente d’antibiotiques est généré par des prescriptions faites en médecine de ville.
Au cours de ces dix dernières années, le nombre de substances antibiotiques disponibles en France a diminué de 15%. Ce solde négatif résulte de l’arrêt de la commercialisation de vingt-cinq substances, alors que seules dix nouvelles substances ou associations de substances ont été commercialisées.
En 2009, les génériques représentaient entre 70% et 80% de la consommation d’antibiotiques en ville. La part des médicaments brevetés dans la consommation est donc désormais très restreinte.
Selon un rapport conjoint de l’ECDC (European Center for Disease Prevention and Control) et de l’EMA (European Medicines Agency), 25 000 patients en Europe seraient morts en 2007 d’infections liées à des bactéries multi-résistantes qui n’ont pu être traitées faute d’antibiotique efficace.
Comment inciter l’industrie pharmaceutique à relancer cette recherche ?
P.C. : Des mesures sont en discussion comme d’augmenter le coût des antibiotiques et de faciliter leur mise sur le marché en simplifiant les démarches, autrement dit en fixant des cadres plus constants, plus cohérents, pour que les règles ne changent pas constamment. Il y a aussi une idée qui serait de prolonger la durée de vie des brevets (vingt ans actuellement) de façon à ce que l’industrie pharmaceutique ait un meilleur retour sur investissement. Car la grande majorité des antibiotiques sont « génériqués », leurs prix de vente ont beaucoup baissé. Tant mieux pour la Sécurité sociale mais, pour la recherche, c’est contre-productif. Car les « génériqueurs » n’investissent pas dans la recherche. C’est par ailleurs une très mauvaise idée de baisser le prix des antibiotiques quand on essaie d’en faire baisser la consommation. Cela va à l’encontre de la lutte contre la dissémination des résistances.
L’essor de la génétique n’a-t-il pas ouvert de nouvelles voies en matière de recherche ?
P.C. : On a pensé aux début des années 90 que l’on allait, grâce à la génomique, trouver de nouvelles cibles, c’est-à-dire de nouveaux modes d’action contre les bactéries, et finalement cela a été très décevant. On a bien identifié des nouvelles cibles mais on n’a pas réussi à développer d’antibiotiques permettant de les attaquer. La majorité des sociétés de biotechnologies qui se sont attaquées à ces questions n’ont pas survécu.
La recherche publique ne peut-elle pallier la démission de l’industrie pharmaceutique ?
P.C. : Il y a des laboratoires académiques qui, du fait de l’absence de recherche dans l’industrie pharmaceutique, se consacrent à ce domaine. Mais le transfert vers l’industrie est un passage obligé car quand vous obtenez une molécule « lead », il faut ensuite mettre en œuvre toute la chimie médicinale : améliorer le principe actif, améliorer la pharmacologie puis réaliser des essais de toxicologie et, enfin, des essais cliniques extrêmement onéreux.
Un autre problème est la faiblesse des forces de pression : je n’ai pas de cohortes de malades avec moi, je n’ai pas de lobby qui puisse faire pression et « booster » la recherche comme cela a été le cas pour le sida par exemple. Lorsqu’un patient fait une maladie nosocomiale à l’hôpital, soit il est mort, soit il est sorti d’affaire (sans que parfois il ait su qu’il avait contracté une infection nosocomiale). Il y a donc peu de chance qu’il milite pour la cause !
L’Organisation mondiale de la santé (OMS) tire la sonnette d’alarme en avançant que sans la mise au point de nouveaux antibiotiques efficaces et avec l’aggravation du phénomène des résistances, le monde pourrait retrouver les conditions qui prévalaient avant les antibiotiques, quand une infection pulmonaire simple pouvait tuer un enfant ou quand les médecins étaient impuissants devant les cas de méningites. Un diagnostic que vous partagez ?
P.C. : Si les choses ne changent pas, c’est effectivement ce vers quoi l’on s’achemine. Des bactéries comme les Acinetobacter (responsables d’infection urinaires et pulmonaires) sont devenues résistantes à tous les antibiotiques. La situation est réellement alarmante.